四省藥監(jiān)局聯(lián)合發(fā)文 新醫(yī)械聯(lián)盟來了
重磅進展,長三角醫(yī)療器械注冊人制度一體化形成。
四省組成,新聯(lián)盟形成
10月29日,據(jù)江蘇省藥品監(jiān)督管理局消息,上海、江蘇、浙江、安徽四地藥監(jiān)局聯(lián)合發(fā)布《長江三角洲區(qū)域醫(yī)療器械注冊人制度試點工作實施方案》。
據(jù)悉,這次的大舉措是按照國家藥品監(jiān)督管理局《關于擴大醫(yī)療器械注冊人試點工作的通知》的要求來進行,以長江三角洲區(qū)域醫(yī)療器械產(chǎn)業(yè)一體化。
由此可以看出,長三角醫(yī)療器械注冊人制度一體化形成。“醫(yī)療器械注冊人制度”這一醫(yī)療器械行業(yè)的創(chuàng)新性的改革,最早從上海試點,后擴大到天津、廣東兩地。
2019年8月,國家藥監(jiān)局相關通知又明確,北京、天津、河北、遼寧、黑龍江、上海、江蘇、浙江、安徽、福建、山東、廣東等21個省、自治區(qū)、直轄市參加醫(yī)療器械注冊人制度試點。
怎么聯(lián)合?有什么影響?
什么是醫(yī)療注冊人制度,經(jīng)歷了怎樣的變革?
此前,在2014年10月起實施的《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》中明確規(guī)定,拿到醫(yī)療器械注冊證才能申請第二類、第三類醫(yī)療器械的生產(chǎn)許可證,而取得生產(chǎn)許可才能生產(chǎn)、受托生產(chǎn)相應醫(yī)療器械。也即把注冊與生產(chǎn)許可捆綁在一起,必須由一個主體來完成。
現(xiàn)在,醫(yī)療器械注冊人制度發(fā)生改革,允許企業(yè)、機構和人員單獨申請醫(yī)療器械注冊證,再以注冊人的身份委托其他企業(yè)生產(chǎn)相應的醫(yī)療器械。即注冊和生產(chǎn)許可可以不由一個主體來完成。
模式變化:
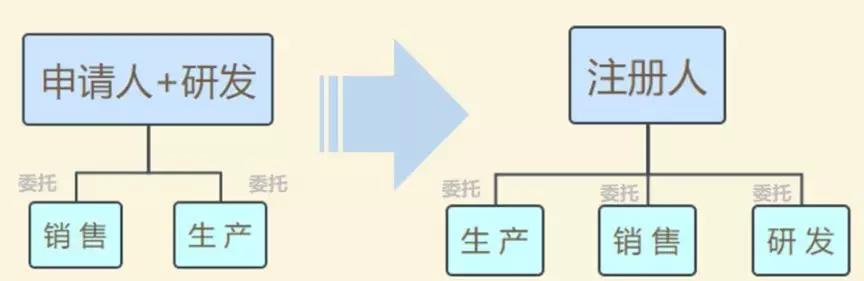
(圖片來源:CFDA法規(guī)在線)
“注冊人制度實現(xiàn)了產(chǎn)品注冊和生產(chǎn)許可的解綁,更利于鼓勵創(chuàng)新、整合社會資源、加快醫(yī)療器械產(chǎn)品上市”,上海市藥監(jiān)局醫(yī)療器械監(jiān)管處處長林森勇認為。
多家企業(yè)初嘗甜頭
在具體落實上,經(jīng)國務院批準,行業(yè)變局由上海開啟。
2018年2月8日,上海遠心醫(yī)療科技有限公司的單道心電記錄儀獲得由上海市藥監(jiān)部門頒發(fā)的第二類醫(yī)療器械產(chǎn)品注冊證,成為國內首個享受到醫(yī)療器械注冊人制度新政的產(chǎn)品。
持有注冊證的遠心醫(yī)療和受托生產(chǎn)的微創(chuàng)電生理都隸屬于上海微創(chuàng),其由此成為我國醫(yī)療器械注冊人制度試點的首個贏家。
上海微創(chuàng)醫(yī)療器械有限公司副總裁李勇說,從我們企業(yè)試點實踐來看,新政大大節(jié)約了研發(fā)成本投入。以我們首個獲得試點注冊證的產(chǎn)品為例,節(jié)約了1000多萬元研發(fā)投入。
嘗到甜頭的上海微創(chuàng),嘗試力度越來越大。截至目前,該企業(yè)已經(jīng)有7家公司12個產(chǎn)品申請注冊人,其中有2個產(chǎn)品已獲得注冊證。
據(jù)悉,除上海微創(chuàng)的2個產(chǎn)品外,上海還有4家企業(yè)6個產(chǎn)品在試點過程中獲批。試點形式還出現(xiàn)了擴大生產(chǎn)場地、多點委托,注冊人為科研型企業(yè)、醫(yī)工互動,非關聯(lián)主體跨區(qū)域委托、進口產(chǎn)品轉國產(chǎn)化等。
美敦力、邁瑞接連響應
醫(yī)療器械注冊人制度可以縮短產(chǎn)品上市周期、提高效率的優(yōu)勢已經(jīng)顯現(xiàn),而且從上海的實踐也能印證,制度改革已經(jīng)為行業(yè)帶來改變,國內醫(yī)械龍頭企業(yè)也接連“啟航”。
就美敦力來說,與上海微創(chuàng)不同的是,美敦力的委托生產(chǎn)方為捷普科技(上海)有限公司,這是一家專業(yè)的第三方代工企業(yè)。以其獲批的手術動力系統(tǒng)為例,委托后,該產(chǎn)品獲批上市僅用了45天的時間。
上海市藥監(jiān)局醫(yī)療器械注冊處處長林峰就此表示,該產(chǎn)品原應作為進口產(chǎn)品注冊,但在試點過程中是本地注冊、本地制造,使得本地化轉移成為可能。該產(chǎn)品上市也意味著將來我國會有更多先進醫(yī)療器械不再通過進口,而是通過本地注冊、生產(chǎn),實現(xiàn)快速上市。
多方期待試點范圍擴大
從目前各地實施的結果來看,注冊人制度試點工作取得一定成效,但還存在一定問題。
比如一些企業(yè)將注冊人制度簡單理解為委托生產(chǎn),沒有意識到注冊人要對醫(yī)療器械全生命周期的質量管理承擔主體責任;有些企業(yè)為享受試點期間的鼓勵政策(如優(yōu)先審評等),刻意拆分出持證人或受托人;部分持有人和委托人之間產(chǎn)生知識產(chǎn)權糾紛等。
需要看到的是,由于目前試點范圍的局限性,醫(yī)療器械注冊人制度雖然不斷釋放紅利,但是速率方面還需加強。
浙江省藥監(jiān)局有關負責人坦言,資本的逐利性決定其會選擇環(huán)境好、成本低的地區(qū)進行生產(chǎn)。上海的生產(chǎn)成本相對較高,注冊人完全可到周邊省份去尋找合作伙伴。尤其是在“將長三角區(qū)域一體化發(fā)展上升為國家戰(zhàn)略”背景下,注冊人試點應拓展到上海周邊省份。
業(yè)內人士就此問題談到,在試點過程中,醫(yī)療器械注冊人應當具備哪些能力或者條件,應當承擔哪些義務;醫(yī)療器械注冊人制度實施會給監(jiān)管帶來哪些挑戰(zhàn),這些挑戰(zhàn)如何破解等問題,還需進一步討論與研究,需要在實踐中不斷探索。
來源:賽柏藍器械



